6 月 8 日,第 52 届欧洲儿科胃肠病学、肝病学和营养学协会(ESPGHAN)会议在格拉斯哥圆满落下帷幕。ESPGHAN 年会是全球儿科胃肠病学、肝病学和营养学领域的顶级学术盛会。作为目前国际上最权威、最具广泛影响力的儿科医学组织,ESPGHAN 今年这场年会汇聚了来自 90 多个国家的 4,500 名专家学者,专家们共同研讨了儿科领域的最新研究热点,并分享了包括肠道微生态、婴儿营养健康、母乳研究等领域的科研成果。

图 1 第 52 届欧洲儿科胃肠病学、肝病学和营养学协会(ESPGHAN)会议
▊ 大咖专家齐交流,聚焦婴儿肠道微生态研究
在本届 ESPGHAN 大会上,肠道微生态是热点议题之一。众所周知,肠道微生态是人体微生态系统的重要组成部分之一,肠道微生态辅助人体进行营养物质的转化与吸收并与多个组织、器官存在密切的相互作用,是人体健康的重要保障。
波士顿儿童医院胃肠病和营养医生、哈佛大学医学院 Jon Vanderhoof 教授就这一议题发表了学术演讲。他表示,肠道微生态对健康至关重要,人体肠道微生物菌群的改变,有可能导致我们更容易过敏或者患上免疫性疾病。为降低罹患此类疾病的风险,可以对菌群进行干预以减少疾病患病风险,而最好的干预时机是在生命早期[1][2]。
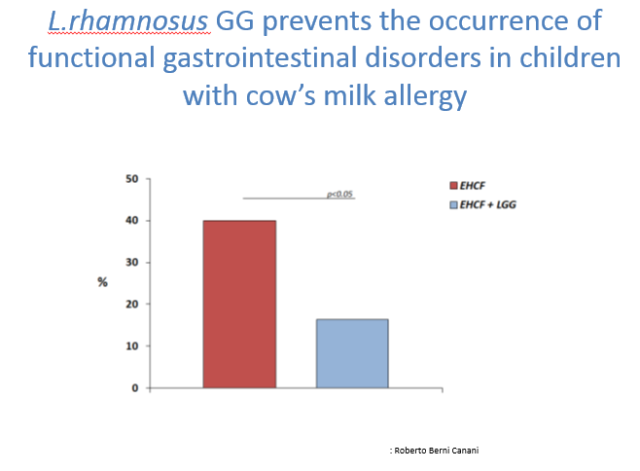
图 2 Jon Vanderhoof 教授,波士顿儿童医院胃肠病和营养医生、哈佛大学医学院高级讲师,报告题目:《Disorders Impacted By the Gut Microbiome Opportunities for Microbiome Manipulation》
一直以来,益生菌作为有益菌的一种,在帮助调节肠道菌群平衡,改善婴幼儿肠道环境方面已有许多探索和实践。在此次大会上,除了 Vanderhoof 教授外,还有学者分享了关于益生菌对坏死性小肠结肠炎的预防起到有效作用的最新研究成果。加之目前益生菌用于幼儿病毒性腹泻和抗生素性腹泻已经有了较为确凿的临床依据,由此看出,益生菌对人体健康的影响是多维度、动态、复杂且广泛的。

图片来源:站酷海洛
▊ 助攻免疫系统「狠」角色,HMO 成大会焦点
除了益生菌,与婴幼儿肠道微生态健康紧密相关的还有另一个重要角色——母乳低聚糖(HMO)。HMO 是母乳中第三大固体成分,含量仅次于乳糖和脂肪。
本次大会上,营养学界对 HMO 的关注依旧高烧不退。来自美国加州大学圣地亚哥分校儿科教授 Lars Bode 博士表示,HMO 与婴儿的健康状态紧密相关,母乳低聚糖可作为益生元影响肠道微生物群的组成,亦可以充当抗黏附剂或受体诱饵阻止病毒、细菌等病原体与上皮细胞表面的糖结合[3][4]。

图 3 Lars Bode 教授,美国加州大学圣地亚哥分校儿科教授,报告题目:《Human Milk Oligosaccharides as primers for the microbiome and immune system》
除了调节肠道微生态之外,HMO 对婴儿自身免疫系统的建立也起到了相当重要的作用。Lars Bode 表示,HMO 能直接调节免疫细胞的相互作用和反应,不仅仅在肠道中,在循环系统和其他组织中也有同样的作用。相关研究表明,母乳中的营养成分可预防过敏症状的发展,其中 HMO 可能担任了很重要的角色。HMO 可以促进有益菌的生长和短链脂肪酸的产生,从而有利于肠道健康和宿主的免疫力[5][6]。
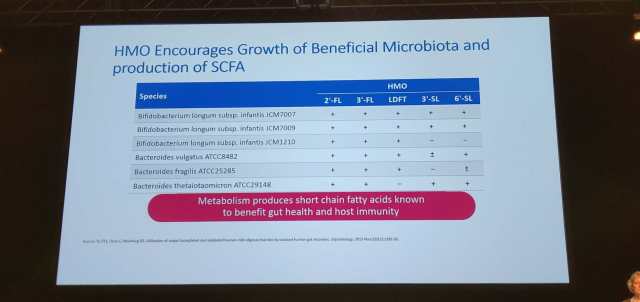
图 4 HMO 可以促进有益菌的生长和短链脂肪酸的产生,从而有利于肠道健康和宿主的免疫力
譬如有学者观察到,母乳中 2-岩藻糖基化乳糖水平与过敏性疾病,如湿疹、IgE 相关性过敏有着显著相关性。2-岩藻糖基化乳糖水平较高时,上述过敏性疾病发生风险较低。有研究者还提出,存在于乳糖-N-岩藻五糖 III(LNFP III)中的 LewisX 抗原可能介导 HMOs 与树突状细胞特异性 ICAM-3 刺激非整合素结合,从而调节婴幼儿对食物的耐受性。较高浓度的 LNFP III 可以减轻牛奶过敏[7]。

图 5 母乳中 2-岩藻糖基化乳糖水平与过敏性疾病,如湿疹、IgE 相关性过敏有着显著相关性
意大利巴里大学儿科学教授 Flavia Indrio 博士在演讲中表示,HMO 有助婴幼儿健康发育已有越来越多证据的支持,通过肠道调节婴儿免疫系统是其较为突出的一个特征[8][9]。

图 6 Flavia Indrio 教授,意大利巴里大学儿科学教授,报告题目:《The exciting potential of prebiotics, postbiotics and HMOs to support the immune system through the gut》
▊ 母乳研究持续发力,营养健康划重点
此次 ESPGHAN 大会上大咖云集,更有很多中国专家远赴欧洲参加,例如合生元营养与护理研究院(BINC)此次便邀请了多名国内专家一同参会。会议结束后,这批专家也向我们分享了他们的参会笔记内容,针对这次会议上关于婴儿营养健康的研究成果,为我们划出了重点。
在会议上,英国伦敦帝国理工学院名誉高级讲师 Rosah Meyer 分享道,母乳喂养有利于远期慢性疾病的预防。母乳中含有各种独特的宏量和微量营成分和生物活性成分,可能会对婴儿健康产生远期影响[10]。
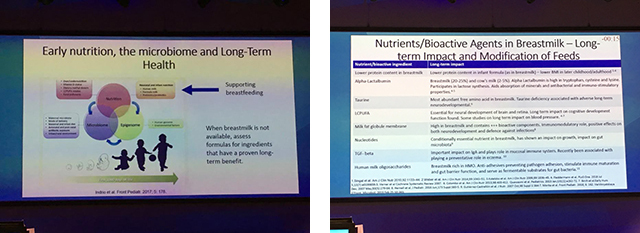
图 7 Rosah Meyer 教授,英国伦敦帝国理工学院名誉高级讲师,报告题目:《The Role of early childhood Nutrition on later life》
对婴儿免疫力有重要影响的母乳成分不止于上文提到的 HMO。实际上,母乳中还天然存在着一种名为骨桥蛋白(OPN)的免疫激活与调节因子,研究表明,该蛋白在婴儿免疫系统的发育和成熟过程中扮演了重要角色。美国伊利诺伊大学香槟分校、加州大学戴维斯分校与复旦大学儿科医院共同完成的骨桥蛋白婴儿临床试验显示,这种蛋白有助于减少体温异常的发生风险[11]。
母乳是宝宝最天然珍贵的营养,被公认为是确保儿童健康和生存的最有效措施之一。数据显示,如果将母乳喂养扩大到全民,每年就可挽救约 82 万名儿童的生命[12],因此对母乳营养的研究一直是营养学界常年的课题。研究表明,母乳中的脂肪能够满足宝宝生长和能量储备的需要,它的重要性无可替代。
需要加以重视的是,尽管世界卫生组织(简称 WHO)推荐母乳喂养宝宝到 2 岁甚至更长时间,但 WHO 同时指出婴儿在生命前六个月应得到纯母乳喂养,以实现最佳生长发育和健康水准。之后,在继续母乳喂养的同时,为满足其越来越高的营养需求,应给婴儿提供营养充足且安全的辅食[13]。

图片来源:站酷海洛
在中国,由于不少妈妈奶水不足,加之女性劳动参与度较高,使得很多家庭母乳喂养难以坚持到 2 岁。这时,可以根据医生建议以及宝宝健康发育的需求,寻找合适的替代产品。比如目前常被谈到的 SN-2 棕榈酸,这种棕榈酸利用了脂肪「改造」技术,与植物油中的棕榈酸结构不同。后者由于饱和脂肪酸棕榈酸处于第 1、3 位上,在肠道水解后会形成游离的棕榈酸与钙结合成钙皂,从而影响钙和脂肪酸的吸收。相反,SN-2 棕榈酸的棕榈酸位于 SN-2 位上,不会游离出来和钙结合,因此更利于婴幼儿营养的吸收。研究表明,SN-2 棕榈酸能显著降低婴儿总皂化脂肪酸排泄量,即 SN-2 棕榈酸有利于婴儿对脂肪酸和钙的吸收[14]。
虽然本次 ESPGHAN 大会已落幕,但是专家学者们的研究还在继续。儿科领域的科研进展关系全球儿童的健康,本次参会的合生元也在持续发力,关注肠道微生态、母乳营养等多个研究领域,期待未来给我们带来更多国际前沿的科学分享。
参考资料:
[1] Vanderhoof J, Mitmesser S. Probiotics in the management of children with allergy and other disorders of intestinal inflammation[J]. Beneficial microbes, 2010, 1(4): 351-356.
[2] Canani R B, Sangwan N, Stefka A T, et al. Lactobacillus rhamnosus GG-supplemented formula expands butyrate-producing bacterial strains in food allergic infants[J]. The ISME journal, 2016, 10(3): 742.
[3] Strandwitz P, Kim K H, Terekhova D, et al. GABA-modulating bacteria of the human gut microbiota[J]. Nature microbiology, 2019, 4(3): 396.
[4] Manthey C F, Autran C A, Eckmann L, et al. Human milk oligosaccharides protect against enteropathogenic Escherichia coli attachment in vitro and EPEC colonization in suckling mice[J]. Journal of pediatric gastroenterology and nutrition, 2014, 58(2): 165-168.
[5] Yu Z T, Chen C, Newburg D S. Utilization of major fucosylated and sialylated human milk oligosaccharides by isolated human gut microbes[J]. Glycobiology, 2013, 23(11): 1281-1292.
[6] Moritz M L, Ayus J C. Misconceptions and barriers to the use of hypertonic saline to treat hyponatremic encephalopathy[J]. Frontiers in Medicine, 2019, 6: 47.
[7] Seppo A E , Sc C A A M , Bode L , et al. Human milk oligosaccharides and development of cow’s milk allergy in infants[J]. J Allergy Clin Immunol, 2017, 139(2):708.
[8] Campeotto F, Suau A, Kapel N, et al. A fermented formula in pre-term infants: clinical tolerance, gut microbiota, down-regulation of faecal calprotectin and up-regulation of faecal secretory IgA[J]. Br J Nutr, 2011, 105(12):1843-1851.
[9] Granier A, Goulet O, Hoarau C. Fermentation products: immunological effects on human and animal models[J]. Pediatric Research, 2013, 74(2):238-44.
[10] Indrio F, Martini S, Francavilla R, et al. Epigenetic Matters: The Link between Early Nutrition, Microbiome, and Long-term Health Development[J]. Frontiers in Pediatrics, 2017, 5:178.
[11] Lönnerdal, Bo, Kvistgaard A S , Peerson J M , et al. Growth, Nutrition, and Cytokine Response of Breast-fed Infants and Infants Fed Formula With Added Bovine Osteopontin[J]. Journal of Pediatric Gastroenterology and Nutrition, 2016, 62(4):650.
[12] Victora C G , Bahl R , Barros, Aluísio J D, et al. Breastfeeding in the 21st century: epidemiology, mechanisms, and lifelong effect[J]. The Lancet, 2016, 387(10017):475-490.
[13] https://www.who.int/features/factfiles/breastfeeding/zh/
[14] Bar-Yoseph F , Lifshitz Y , Cohen T , et al. SN2-Palmitate Reduces Fatty Acid Excretion in Chinese Formula-fed Infants[J]. Journal of Pediatric Gastroenterology and Nutrition, 2016, 62.
文章来源:合生元
图片来源:拍摄于第 52 届 ESPGHAN 现场
