脐带血是胎儿娩出断脐后从脐静脉中采集获得的血液,其中因含有丰富的造血干细胞、间充质干细胞、淋巴细胞等多种类细胞,已经成熟应用于多种血液系统疾病、免疫系统疾病、部分恶性肿瘤疾病等的治疗之中,并取得不错的效果。在 2022 年北京地区妇产科学专业学术年会上,来自北京大学第三医院生殖医学中心朱小辉教授就详细讲解了胚胎植入前遗传学检测(PGT)联合 HLA 配型技术在脐带血临床治疗中的应用。
目前在我国,罕见病患者超过了 2000 万,其中 80% 都是由遗传缺陷引起,以单基因遗传病最为多见。目前已知的单基因病约 7000 种,50% 以上会在新生儿或者儿童阶段发病,大部分致畸、致残甚至致死,为社会和家庭带来沉重的负担。而面对此类遗传疾病,几乎毫无办法,个别疾病就算有药可用,也是天价,一般的家庭无力承受。
因此对于遗传性罕见病,防患于未然是最好的选择。WHO 针对遗传疾病提出了三级预防的策略,分别为第一级孕前,第二级孕中,第三级新生儿。相比新生儿出生后的第三级预防改善出生缺陷患儿的病情来说,一级和二级的预防是更加有效的阻断患儿出生的方法。常规产前诊断属于二级预防,而单基因胚胎着床前遗传学检测(PGT)可以很大程度的减少孕妇因产前诊断在孕中期出现引产的痛苦。
单基因病胚胎着床前遗传学检测(PGT)技术及应用
PGT 的基本流程为,精子卵子在体外受精后发育成胚胎,然后通过 PGT 活检其中的少量细胞,将检测后健康正常的胚胎植入母体,从而诞生健康后代。这项技术可以应用于单基因病、染色体病、遗传筛查等等。而根据检测目的不同,我们将 PGT 检测又分为 PGT-A(染色体非整倍性 PGT),PGT-SR(染色体结构重排 PGT),PGT-M(单基因病 PGT),PGT-HLA(人类白细胞抗原 PGT)。本次会议主 要分享了 PGT-M 和 PGT-HLA 两种检测技术。
在 PGT-M 的临床步骤中,疾病诊断、基因检测、遗传咨询是最关键的部分,它影响到检测的最终结果。PGT 检测中运用 IVF(体外受精)技术获得受精卵,在胚胎时期取活检样本作为遗传诊断的样本。这一阶段的活检方法分为极体活检、卵裂球活检、滋养外胚层活检和囊胚腔液活检。目前多采用安全性最高、更为准确的滋养外胚层活检。
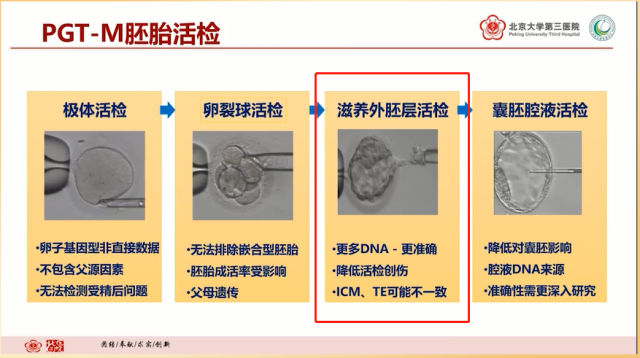
PGT-M 检测在显微环境下取下活检的细胞团,利用酶的作用分解成单个细胞,再将质地均匀、状态完整的细胞用于胚胎检测,最大程度的减少因为细胞状态不一而造成的误差。由于是基于单个细胞基础上进行的活体检测,所以相比多细胞水平基因检测难度更大。人类一毫升的血液中就有百万数量级的细胞,多细胞水平基因检测就相当于在鱼塘里捞鱼,而单细胞水平基因检测就相当于在一个湖里抓仅有的一条鱼,因此如何捞上这条鱼就成了 PGT 技术中的关键所在。
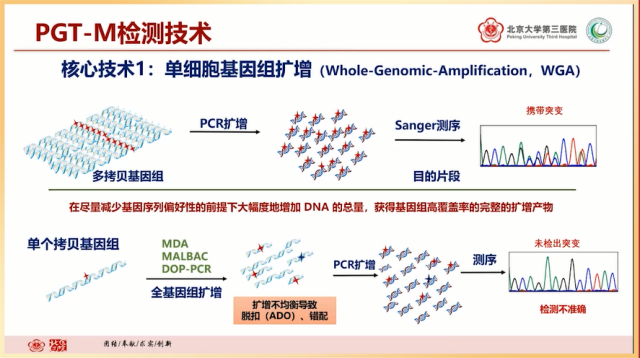
首先用到的核心技术就是单细胞基因组扩增(WGA),即通过 PCR 技术,可以把细胞的目的片段部分复制百万倍。但是无论是什么样的扩增方法,都有提取不均衡所导致的脱扣现象,就会出现基因片段某些区域扩增多,某些区域扩增少,导致检测不准确。
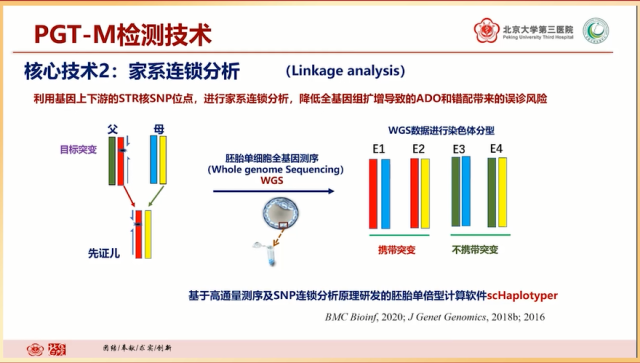
因此解决这种问题就应用到第二个核心技术——家系连锁分析。在突变位点无法看到,但致病基因上下游 STR 和 SNP 位点很丰富,通过胚胎单细胞的全基因测序,测出的数据中已经富含了 SNP 的连锁标记信息,再通过连锁标记就能对携带患病基因的染色体分型。而高通量测序的数据,再通过自主研发的胚胎单倍型计算软件进行分析,就可以准确地得到这个胚胎是否存在突变和致病基因。
通过整合上述技术,将整个胚胎检测策略称为 MARSALA,简单来说就是将从活检胚胎上取下的单细胞,通过全基因组扩增,再通过高通量测序,经由数据分析后,一次测序得到单基因突变位点检测结果、染色体非整倍性检测结果和 SNP 连锁分析结果三种信息。这种检测策略扩大了诊断适应症,包括无先证者家系和常规检测手段误诊率高的疾病,并且提高诊断准确率的同时降低了检测成本。
应用 MARSALA 这个策略,除了进行大量的单基因病诊断之外,还可以进行 HLA 配型分析。PGT-HLA 技术可以适用于孩子后天发生的血液疾病和免疫疾病,凡是可以用干细胞方法治疗的疾病,都是 PGT-HLA 适合检测的适应症。
HLA(human leukocyte antigen,人类白细胞抗原) 是人类主要组织相容性复合体(MHC)的表达产物,HLA 的基因簇位于 6p21,此基因簇是目前所知道的人体最复杂的多肽系统。其中 HLA-A,HLA-B,HLA-C,HLA-DR 这四个亚簇是对器官和干细胞移植密切相关的。
2000 年时,世界首例通过 PGT-M\HLA 技术的宝宝出生于一个患有范可尼贫血的家庭,当时使用特异引物巢氏 PCR 和 STR 连锁的方法,而这种方法的缺点是不能特别准确的判断基因簇附近和基因簇内部的染色体 SNP 现象,而应用 MARSALA 则可以完美的解决 HLA-SNP 连锁分型这个问题。
来自北医三院的临床应用案例:
患者家庭遗传有粘多糖贮积症的致病基因,患儿为粘多糖贮积症Ⅳ型。该病由于粘多糖贮积在患儿体内,导致骨发育异常,同时还累积到患儿心脏以及呼吸系统,未经治疗的患儿仅能存活到儿童期或者青少年期。基因检测结果显示这个患儿在 GALNS 携带有两个致病性变异位点,分别来自于他们的父母,是一个常染色体隐性遗传病。GALNS 位点所影响的正是身体合成的一种溶酶体酶,这种溶酶体酶的缺失导致身体缺乏可以代谢粘多糖的能力,从而患病。这种疾病治疗方法少,却是造血干细胞治疗的适应症之一。

患儿家庭就诊时正处于很困难的时期,因为此疾病适合造血干细胞移植的时机是 3 岁之前,患儿此时已经接近 2 岁,患儿的父母咨询过全国七大脐血库和国内及台湾骨髓库,都没有找到合适的造血干细胞源,如果利用二胎的造血干细胞来治疗的话,与患儿 HLA 全相合并且健康的概率仅有 18%。所以利用 PGT-M\HLA 技术对于这个家庭而言是一个最佳的解决方案。
经过第一个周期,得到了 4 枚胚胎,通过检测得到染色体拷贝数变异的结果,在 4 个胚胎中,1、2、3 号都是染色体未见异常,4 号胚胎出现异常。而基因突变位点检测发现,胚胎 1、2、3、4 都杂合携带父母其中一方的突变,但都是健康的胚胎。通过 HLA 分型,胚胎 1 和 2 与患儿是全相合的,所以这个家庭非常幸运,在第一个周期就获得了两枚适合移植的胚胎。最终使用胚胎 1 成功妊娠。孕中期羊水检测显示胎儿与患儿 HLA 配型成功,全相合。

在各个科室做好一切准备之后,2019 年 9 月 20 日宝宝出生,产科立刻采集了脐带血,转移至北京市脐血库进行制备、检测、程序化冻存,等待患儿做好移植准备。在 2019 年 11 月 22 日,患儿接受了弟弟的脐带血移植治疗。经过一个月,患儿成功出仓,四个月后,患儿的酶学水平恢复正常。

PGT 有自己的独特特点,首先,它具有时效性,因此对患儿的疾病进展和治疗时机要求严格;其次是女方的年龄,女方年龄过大,妊娠成功率更低。除此之外,还要考虑夫妻是否有 IVF(体外受精)的禁忌症等等;但是最主要的还是这种检测策略需要多个学科的合作,比如血液科,儿科,产科,生殖临床,IVF 实验室,分子遗传实验室还有脐血库的通力合作。
PGT-HLA 适用症广泛,检测精准,在获得健康后代的同时,还可以得到全相合的干细胞源,一举两得。因此该技术可以在临床上广泛推广应用,从而惠及更多的家庭。希望 PGT 这项技术可以帮助到越来越多具有罕见病的家族摆脱困扰,也希望更多的人了解 PGT 技术,让遗传病不再是困扰人类的顽疾,让更多的患病家庭找到希望。
* 讲者介绍

朱小辉 副主任技师
北京大学第三医院遗传中心分子遗传实验室组长
北京大学第三医院生殖中心国家妇产科疾病研究中心、北京市及教育部重点实验室实验室主管
主要专业方向:
单基因遗传病基因检测、产前诊断及胚胎着床前遗传学检测(PGT)
发表 SCI 论文 30 余篇
